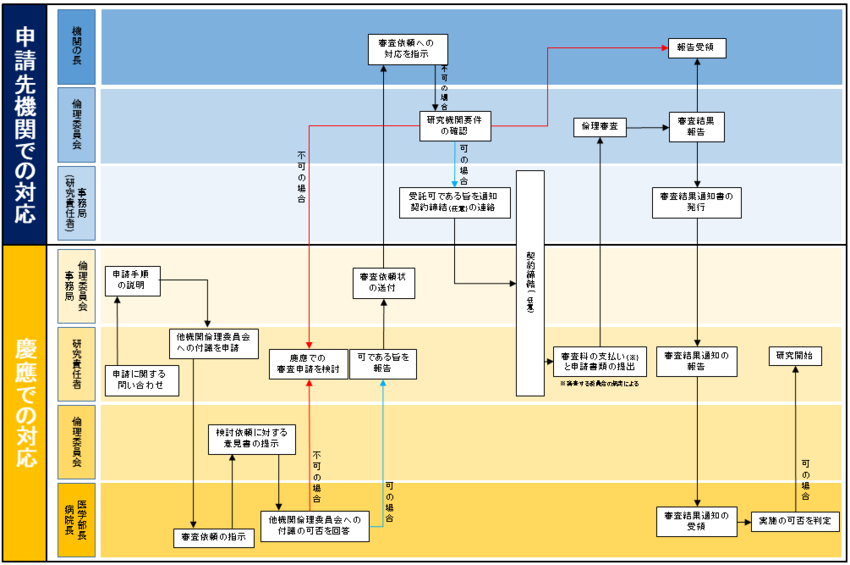
外部の倫理審査委員会で審査を受ける場合の手順について(旧指針)
1.医学部長・病院長(慶應)へ、外部の倫理審査委員会に審査を委託することの検討依頼
人を対象とする医学系研究に関する倫理指針(旧指針)に基づく研究に、これから外部の倫理審査委員会へ審査を委託するためには、事前に医学部長・病院長の了承を得る必要があります。学術研究支援課(研究倫理担当)med-rinri-ft_pt@adst.keio.ac.jpへ各種資料(以下1~5)をご提出ください。| 資料名 | 備考 | |
|---|---|---|
| 倫理審査検討依頼書 | 記入し押印のうえ院内便にてご提出ください。 | |
| 研究計画書 | 審査委託先の倫理審査委員会で、「審査予定」のものをご提出ください。 | |
| 説明文書・同意書またはオプトアウト文書 | ||
| 審査委託先の倫理審査委員会を設置する機関の長宛の倫理審査依頼書 | 審査委託先の委員会事務局等がひな型を用意しているかと思われますので、適宜確認のうえ、ご提出ください。 | |
| その他参考資料 | 上記2,3,4の資料以外に入手している書類がございましたら、適宜ご提出ください。 |
2.医学部長・病院長(慶應)から、審査委託可否の回答
審査が行われる予定の倫理審査委員会への審査委託の可否について、医学部長・病院長による決裁をふまえ、学術研究支援課(研究倫理担当)より回答します。資料提出から審査委託可否の回答まで、およそ4週間を要します。3.審査委託先の倫理審査委員会へ審査依頼
学術研究支援課(研究倫理担当)より、審査する倫理審査委員会がある機関の長宛の倫理審査依頼書(公印押印済)を申請者へお送りします。申請者側にて審査委託先の倫理審査委員会事務局等と審査手続きをお進めください。なお審査委託先の倫理審査委員会等からの指示があった場合、審査依頼とあわせて審査業務の委受託契約を結ぶ必要がありますので、その際は別途学術研究支援課(研究倫理担当)med-rinri-ft_pt@adst.keio.ac.jpにご相談ください。
4.審査委託先の倫理審査委員会での承認判定後、医学部長・病院長(慶應)へ研究実施許可申請
審査委託先の倫理審査委員会で審査され、承認と判定されましたら、学術研究支援課(研究倫理担当)med-rinri-ft_pt@adst.keio.ac.jpへ各種資料(以下1~6)をご提出ください。| 資料名 | 備考 | |
|---|---|---|
| 倫理審査結果通知書 | 承認された審査結果通知書をご提出ください。 | |
| 研究実施許可申請書 | 必要箇所を入力し作成してください。 | |
| 研究計画書 | 承認された研究計画書をご提出ください。 | |
| 説明文書・同意書またはオプトアウト文書 | 承認された書式から、書式内の機関名や問い合わせ先等の情報を適宜慶應での実施に適した内容に修正のうえ、ご提出ください。 (必ず事前に、研究代表者に修正が可能かご確認ください) |
|
| 利益相反事項開示書 利益相反事項開示書(別紙) |
必要箇所を入力し作成してください。 | |
| 慶應義塾大学病院臨床研究利益相反マネジメント委員会(以降、COI委員会)への補足情報 | ひな型にある記載例にならって入力してください。 |
※再度審査委託先の倫理審査委員会で倫理審査が行われて研究計画に変更が出たり、慶應内での実施体制(分担者の変更等)が発生した場合には、都度医学部長・病院長(慶應)へ研究実施許可申請が必要となります。その場合の手続きはこちらの研究実施許可申請から開始することになり、提出資料は上の1~6となります。
注)慶應内での実施体制(分担者の変更等)が発生したのみ(審査委託先の倫理審査委員会で審査が行われていない)の研究実施許可申請においては、「1 倫理審査結果通知書」は不要となります。
5.医学部長・病院長(慶應)からの研究実施許可
審査委託先の倫理審査委員会にて承認されたことを医学部長・病院長へ報告し、慶應における研究実施について許可がおりましたら、学術研究支援課(研究倫理担当)より回答します。なお、研究責任者(研究グループは)実施許可の連絡を受けてから、研究開始となります。上記手続きのフロー図(旧指針)